国家药品监督管理局关于14批次药品不符合规定的通告
(2018年第63号)
经吉林省药品检验所等6家药品检验机构检验,标示为陕西汉王药业有限公司等13家企业生产的14批次药品不符合规定。
涉及的标示生产企业、不合格产品
经河北省药品检验研究院检验,标示为江西德成制药有限公司生产的1批次复方醋酸地塞米松乳膏不符合规定,不符合规定项目包括含量测定、装量。
经吉林省药品检验所检验,标示为陕西汉王药业有限公司生产的2批次木香顺气丸不符合规定,不符合规定项目为性状。
经山西省食品药品检验所检验,标示为河北仁心药业有限公司、江西樟树成方中药饮片有限公司、永州市永靛中药饮片有限公司、廉江市华晟中药饮片有限公司、广西贵港市绿之源种养发展有限公司中药饮片厂、张掖市恒利中药材加工有限公司生产的6批次羌活不符合规定,不符合规定项目包括性状、含量测定、浸出物。
经湖南省药品检验研究院(湖南药用辅料检验检测中心)检验,标示为四川子仁制药有限公司生产的1批次石淋通颗粒不符合规定,不符合规定项目为溶化性。
经湖南省药品检验研究院(湖南药用辅料检验检测中心)检验,标示为赤峰维康生化制药有限公司、甘肃省西峰制药有限责任公司生产的2批次维U颠茄铝胶囊不符合规定,不符合规定项目为含量测定。
经北京市药品检验所检验,标示为健民药业集团股份有限公司生产的1批次小金胶囊不符合规定,不符合规定项目为微生物限度。
经海南省药品检验所检验,标示为浙江惠迪森药业有限公司生产的1批次注射用拉氧头孢钠不符合规定,不符合规定项目为有关物质。
处置情况
对上述不符合规定药品,相关药品监督管理部门已采取查封、扣押等控制措施,要求企业暂停销售使用、召回产品,并进行整改。
国家药品监督管理局要求相关省级药品监督管理部门对上述企业和单位依据《中华人民共和国药品管理法》第七十三、七十四、七十五条等规定对生产销售假劣药品的违法行为进行立案调查,自收到检验报告书之日起3个月内完成对相关企业或单位的调查处理并公开处理结果。
附件
14批次不符合规定药品名单 (可在澎湃APP内点击查看大图)
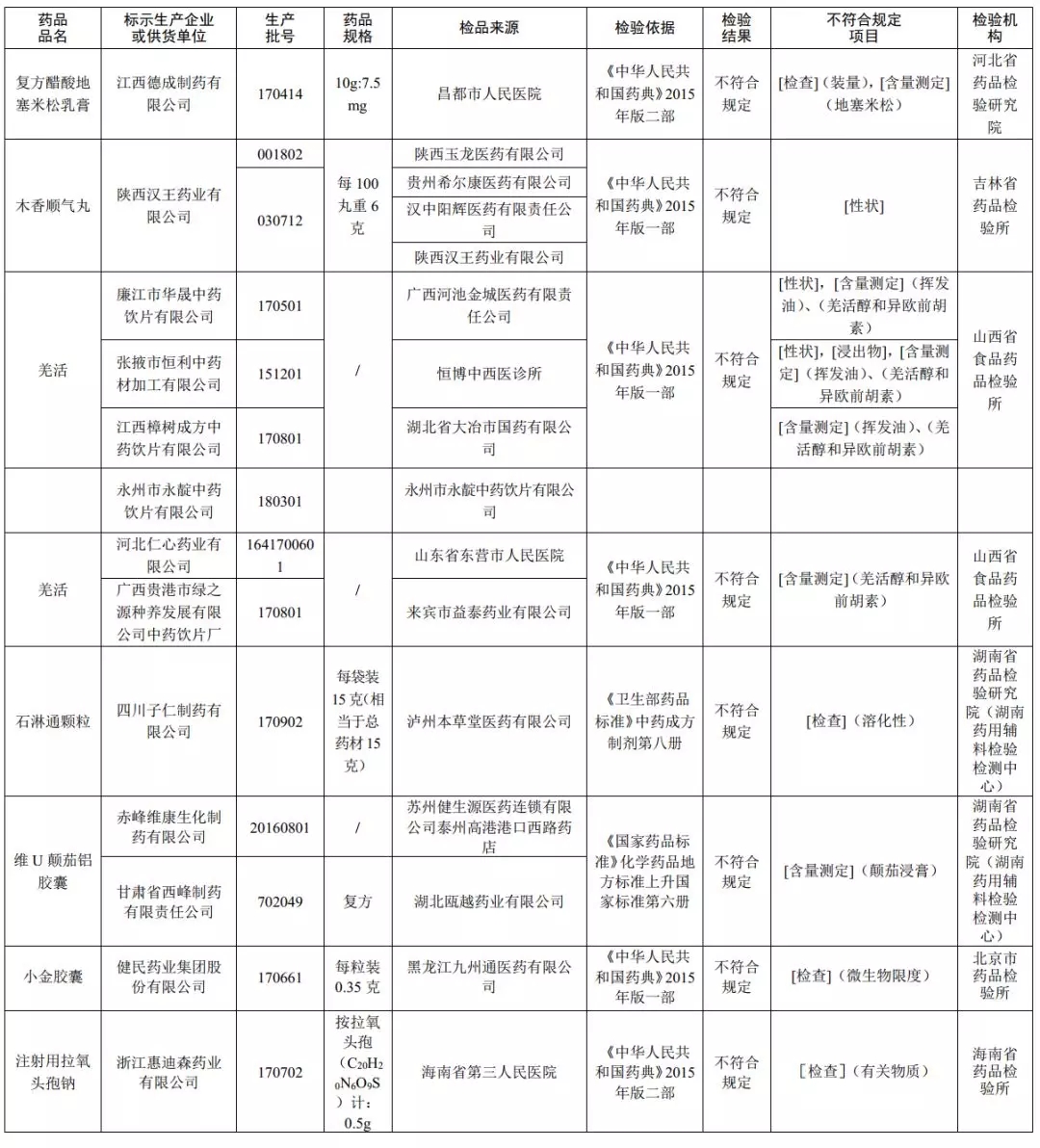

不符合规定项目的小知识
1.药品标准中的性状项记载药品的外观、臭、味、溶解度以及物理常数等,在一定程度上反映药品的质量特性。性状不符合规定可能与投料质量及工艺、储运环境等因素有关,往往直接影响药品质量。
2.药品标准中的检查项包括反映药品的安全性与有效性的试验方法和限度、均一性与纯度等制备工艺要求等内容;对于规定中的各种杂质检查项目,系指该药品在按既定工艺进行生产和正常贮藏过程中可能含有或产生并需要控制的杂质(如残留溶剂、有关物质等);改变生产工艺时需另考虑增修订有关项目。检查项下根据不同药品的特性有有关物质、微生物限度、装量、溶化性等分项目。
有关物质系指药品中的有机杂质,是反映药品纯度、保证用药安全的重要指标之一。药品中的有关物质主要有两个来源:一是由制备过程中带入的杂质,例如原料不纯、部分原料反应不完全、反应过程中产生的中间体或副产物在精制时没有除尽;二是药品在贮存或运输中,由于贮存时间过长,包装保管不善,在外界条件(如日光、空气、温度、湿度等因素)的影响或微生物的作用下,导致药品本身发生降解产生的杂质。在药品的质量标准中,对存在的无毒、低毒或高毒性的杂质都制定了严格的指标。有关物质不符合规定,可能会对药品安全性带来影响。
微生物限度系对非直接进入人体内环境的一大类药物制剂的微生物控制要求。由于此类制剂用药的风险略低,可以允许一定数量的微生物存在,但不得检出一些条件致病菌。因此,微生物限度分为计数检查和控制菌检查两部分。计数检查通常由需氧菌总数或(和)霉菌和酵母菌总数组成,控制菌检查根据给药途径的风险分设不同的致病菌检查项目。
装量系反映药品重量或容量的指标,适用于固体、半固体、液体制剂。除制剂通则中规定检查重(装)量差异的制剂及放射性药品外,按最低装量检查法进行检查,包括重量法和容量法。装量不符合规定会导致临床给药剂量不足,带来相应风险,不符合规定的主要原因是工艺控制不当。
溶化性系反映药品在规定时间内溶化情况的指标,适用于颗粒剂、茶剂、含片等制剂。溶化性不符合规定会影响药品的吸收,或说明药品中含有不溶性杂质,可能与原辅料质量、工艺控制等有关。
3.药品标准中的含量测定项系指用规定的试验方法测定原料及制剂中有效成分的含量,一般可采用化学、仪器或生物测定方法。含量测定与药物的疗效相关。含量测定不符合规定与投料量、投料质量及工艺等有关。
编辑:燕青 来源:国家药品监督管理局